Il faut s’imaginer un mélange harmonieux d’ADN et d’algortihmes, une mélodie inattendue de bases azotés et bytes sur octets, tournant sur des disques magnétiques plutôt que sur boite de pétri. Le maestro responsable de cet assemblage baroque est une nouvelle science aux pouvoir aussi puissants qu’émergeants : la bioinformatique. Fin 2020, la bioinformatique apparaît sous les projecteurs pour grand public. Google avait annoncé que son intelligence artificielle AlphaFold avait résolu l’un des problèmes les plus importants de la biologie : le repliement des protéines. Mais de quoi s’agit-il ?
La compréhension de la structure tridimensionnelle des protéines est cruciale pour la recherche en biologie et la conception de médicaments. Jusqu’à récemment, la détermination expérimentale de ces structures était une tâche ardue et chronophage. Cependant, AlphaFold, développé par DeepMind, a émergé comme un pionnier dans le domaine de la prédiction des structures protéiques en utilisant l’intelligence artificielle.
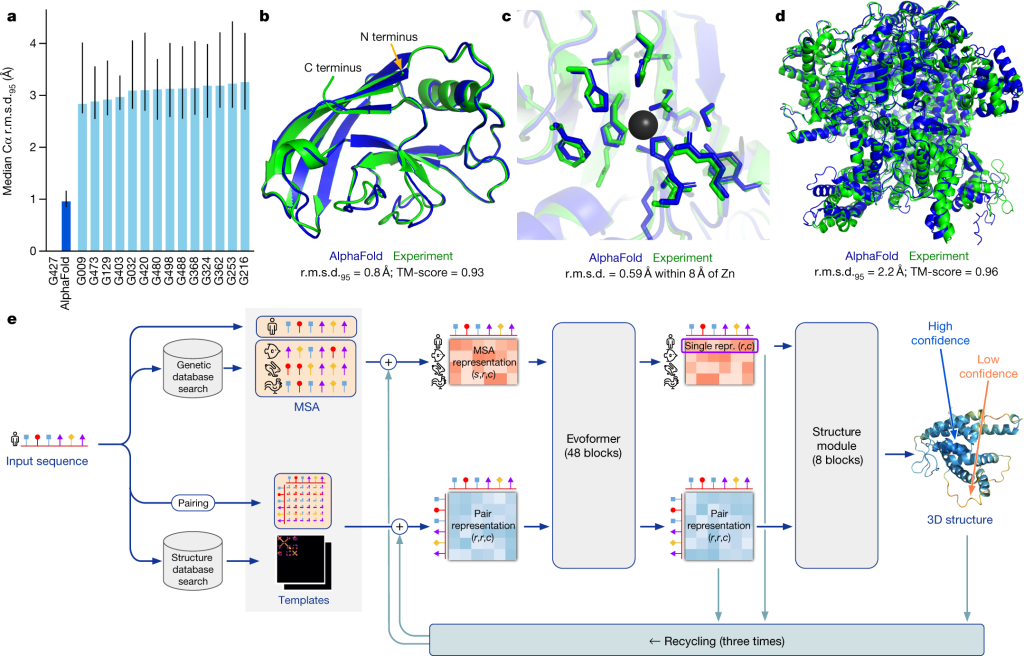
Source : Jumper, J., Evans, R., Pritzel, A. et al. Highly accurate protein structure prediction with AlphaFold. Nature 596, 583–589 (2021). https://doi.org/10.1038/s41586-021-03819-2
Comment fonctionne AlphaFold ?
AlphaFold est basé sur des réseaux neuronaux profonds, une forme d’intelligence artificielle, qui a la capacité d’apprendre à partir de données. Les chercheurs ont nourri le modèle avec une immense quantité de données sur les structures protéiques connues, ainsi que sur les séquences d’acides aminés qui les composent. En utilisant ces données, AlphaFold est capable de prédire la structure tridimensionnelle d’une protéine donnée.
Le modèle AlphaFold fonctionne en deux étapes principales. Tout d’abord, il prédit la distance entre chaque paire d’acides aminés dans la protéine, ce qui permet de déterminer la disposition spatiale des atomes. Ensuite, il ajuste cette prédiction pour obtenir une structure tridimensionnelle plus précise. Les prédictions d’AlphaFold sont ensuite évaluées à l’aide de diverses mesures de qualité pour déterminer leur fiabilité.
L’impact d’AlphaFold
AlphaFold a eu un impact majeur sur la recherche en biologie et dans de nombreux domaines connexes. Sur son tableau de chasse, deux réussites de poids : En 2021, une équipe de scientifiques a utilisé AlphaFold pour prédire la structure de la protéine SARS-CoV-2, le virus responsable de la COVID-19. Cette découverte a permis aux scientifiques de développer de nouveaux vaccins et traitements contre la maladie. En 2022, une équipe de scientifiques a utilisé AlphaFold pour prédire la structure de la protéine tau, une protéine impliquée dans la maladie d’Alzheimer. Cette découverte a permis aux scientifiques de comprendre comment la protéine tau s’accumule dans le cerveau des personnes atteintes de la maladie, et d’identifier de nouvelles cibles pour le développement de traitements.
L’un des domaines les plus prometteurs est la conception de médicaments. En comprenant la structure des protéines cibles responsables de maladies, les chercheurs peuvent développer des médicaments plus ciblés et efficaces. De plus, AlphaFold a le potentiel de révolutionner la biologie structurale en fournissant des informations précieuses sur des protéines jusqu’alors non caractérisées, et ce en évitant le passage par l’expérimentation animale qui a mauvaise presse auprès du grand public.
Sources :
- Jumper, J., et al. (2021). Highly accurate protein structure prediction with AlphaFold. Nature, 596(7873), 583-589.
- Senior, A. W., et al. (2020). Improved protein structure prediction using potentials from deep learning. Nature, 577(7792), 706-710.
- AlphaFold – DeepMind. (https://deepmind.com/research/case-studies/alphafold)


Laisser un commentaire